ATAXIA
What is Ataxia?
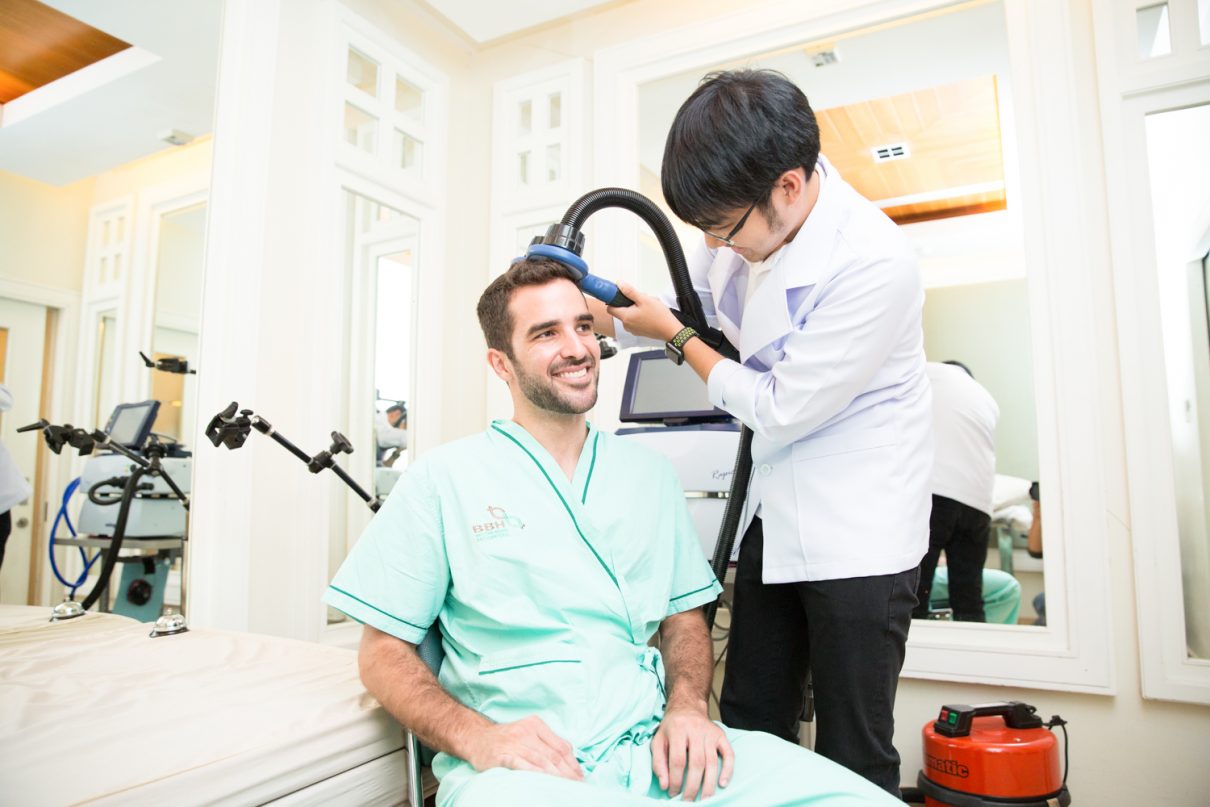
Ataxia is a degenerative disease of the nervous system particularly in the cerebellum, the part of the brain that controls the coordination of movement. Damage to the cerebellum and degeneration or loss of nerves cells brings about this condition.
What causes Ataxia?
Common causes of Ataxia are the following:
- Hereditary – a defect in a certain gene that makes abnormal proteins. The abnormal proteins hamper the function of nerve cells, primarily in your cerebellum and spinal cord, and cause them to degenerate.
- Head trauma
- Stroke – severe reduction or interruption of blood flow to the brain, depriving the brain tissue of oxygen and nutrients
- Cerebral palsy
- Autoimmune diseases – examples are Multiple Sclerosis, Sarcoidosis, celiac disease and others
- Tumor – A growth on the brain, cancerous (malignant) or noncancerous (benign), can damage the cerebellum
- Alcohol and drug intoxication, heavy metal poisoning
Signs and Symptoms of Ataxia
Ataxia symptoms vary by person as well as rate of progression. Symptoms may worsen slowly, over decades or quickly, over a few months.
- Poor coordination
- Slurred speech
- Difficulty eating and swallowing
- Deterioration of fine motor skills such as feeding self or buttoning a shirt
- Unsteady gait, difficulty walking
- Abnormalities in eye movements
- Tremors
Role of Functional Medicine in Ataxia
Functional Medicine aims to support the patient in improving their quality of life through an individualized approach. And since Ataxia results from many possible causes, a thorough investigation of underlying triggers and other related conditions is done to come up with the best possible treatment plan addressing the specific needs of the patients. Apart from nutrition modification and supplementation, Ataxia responds well to intensive physical therapy, Hyperbaric Oxygen Therapy, Fecal Microbiota Transplantation for gastric problems, and DFPP.
Please click here to send us inquiry for free online consultation with our medical team.
- Published in Neurological Rehabilitation Center, Services
Traumatic Brain Injury
การบาดเจ็บที่ศีรษะ
การบาดเจ็บที่ศีรษะโดยปกติเป็นผลมาจากการกระแทกอย่างรุนแรง หรือมีแรงมากระแทกที่ศีรษะหรือร่างกาย วัตถุที่แทรกซึมเข้าสู่เนื้อเยื่อสมอง เช่น กระสุนหรือชิ้นส่วนของกะโหลกศีรษะแตกก็อาจเป็นสาเหตุทำให้สมองบาดเจ็บได้ สมองบาดเจ็บที่ไม่รุนแรงอาจส่งผลกระทบต่อเซลล์สมองของคุณชั่วคราว การบาดเจ็บที่สมองอย่างรุนแรงมากสามารถทำให้เกิดแผลช้ำ, เนื้อเยื่อฉีกขาด, เลือดออก และเกิดความเสียหายทางกายภาพอื่นๆ ในสมองได้ การบาดเจ็บเหล่านี้อาจส่งผลให้เกิดภาวะแทรกซ้อนในระยะยาว หรือการเสียชีวิตได้
อาการ
สมองบาดเจ็บสามารถส่งผลกระทบต่อร่างกายและจิตใจที่หลากหลาย อาการหรืออาการแสดงบางอย่างอาจปรากฏขึ้นทันทีหลังเกิดภยันตราย ในขณะที่คนอื่นอาจปรากฏวันหลังหรือสัปดาห์ต่อมา
สมองบาดเจ็บไม่รุนแรง
อาการและอาการแสดงของสมองบาดเจ็บที่ไม่รุนแรง อาจรวมถึง:
● อาการทางกายภาพ เช่น การขาดสติสัมปชัญญะสองสามวินาที, ไม่กี่นาที, ไม่สูญเสียความรู้สึกตัว แต่ยังมีความงุนงง, สับสน หรือการรับรู้สภาพแวดล้อมผิดปกติ, ปวดหัว, 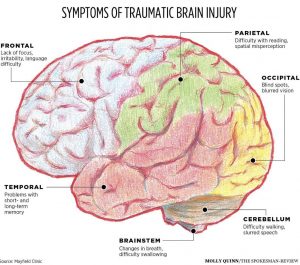 คลื่นไส้ หรืออาเจียน, อ่อนเพลียหรือง่วงนอน, มีปัญหาในการพูด, นอนหลับยาก, นอนหลับมากกว่าปกติ, เวียนศีรษะหรือสูญเสียการทรงตัว
คลื่นไส้ หรืออาเจียน, อ่อนเพลียหรือง่วงนอน, มีปัญหาในการพูด, นอนหลับยาก, นอนหลับมากกว่าปกติ, เวียนศีรษะหรือสูญเสียการทรงตัว
● อาการทางประสาทสัมผัส เช่น ปัญหาระบบประสาทสัมผัส, ความไวต่อแสงหรือเสียง, มีอาการด้านพุฒิปัญญาหรืออาการทางจิต, มีปัญหาความจำหรือสมาธิ, มีการเปลี่ยนแปลงทางอารมณ์ หรืออารมณ์แปรปรวน, รู้สึกหดหู่ หรือวิตกกังวล
สมองบาดเจ็บในระดับปานกลางจนถึงอย่างรุนแรง
สมองบาดเจ็บในระดับปานกลางจนถึงขั้นรุนแรงอาจรวมถึงอาการและอาการแสดงอื่นๆ ของสมองบาดเจ็บที่ไม่รุนแรง เช่นเดียวกับอาการเหล่านี้ที่อาจปรากฏขึ้นภายในชั่วโมงแรกจนถึงวันหลังจากได้รับบาดเจ็บที่สมอง
อาการในเด็ก
ทารกและเด็กเล็กที่มีอาการบาดเจ็บที่ศีรษะ อาจไม่สามารถสื่อสารกับอาการปวดหัว, ปัญหาประสาทสัมผัส, ความสับสน และอาการคล้ายกัน ในเด็กที่มีอาการบาดเจ็บที่ศีรษะ คุณอาจสังเกตเห็นการเปลี่ยนแปลงในพฤติกรรมการกินหรือนิสัยการกิน, หงุดหงิดง่ายหรือผิดปกติ, ง่ายร้องไห้ไม่หยุดและไม่สามารถปลอบได้, เปลี่ยนแปลงความสามารถในการใส่ใจ, เปลี่ยนนิสัยการนอนหลับ, ชัก, เศร้าเสียใจหรือซึมเศร้า, ง่วงนอน, การสูญเสียความสนใจในของเล่นที่ชอบหรือกิจกรรมที่โปรดปราน
สาเหตุ
การบาดเจ็บที่ศีรษะมักเกิดจากการกระแทกหรือการบาดเจ็บอื่นๆ ที่บริเวณศีรษะหรือร่างกาย ระดับความเสียหายขึ้นอยู่กับปัจจัยหลายประการ รวมถึงลักษณะของการบาดเจ็บและแรงกระแทก เหตุการณ์ทั่วไปที่ทำให้เกิดการบาดเจ็บที่ศีรษะ เช่น การล้ม, การชนที่เกี่ยวข้องกับยานพาหนะ, ความรุนแรง, การบาดเจ็บจากกีฬา, การระเบิด และการบาดเจ็บจากการต่อสู้อื่น ๆ
ปัจจัยเสี่ยง
ผู้ที่มีความเสี่ยงต่อการบาดเจ็บที่ศีรษะมากที่สุด ได้แก่ :
● เด็ก โดยเฉพาะทารกแรกเกิดถึงเด็กอายุ 4 ปี
● คนหนุ่มสาว โดยเฉพาะผู้ที่มีอายุระหว่าง 15 และ 24
● ผู้ใหญ่อายุ 60 ปีขึ้นไป
● เพศชายในทุกช่วงอายุ
ภาวะแทรกซ้อน
ภาวะแทรกซ้อนหลายอย่างสามารถเกิดขึ้นได้ทันทีหรือในไม่ช้าหลังจากได้รับบาดเจ็บที่ศีรษะ การบาดเจ็บที่รุนแรงเพิ่มความเสี่ยงของจำนวนที่มากขึ้นและภาวะแทรกซ้อนที่รุนแรงมากขึ้น รวมทั้ง
● การเปลี่ยนแปลงสติ
● ภาวะแทรกซ้อนทางกายภาพ
● ปัญหาทางปัญญา
● ปัญหาการสื่อสาร
● การเปลี่ยนแปลงพฤติกรรม
● การเปลี่ยนแปลงทางอารมณ์
● ปัญหาทางประสาทสัมผัส
● โรคสมองเสื่อม
แผลผ่าตัด
เมื่อพูดถึง TBI มักใช้คำว่า “mass lesion” นี่หมายถึงบริเวณที่มีการบาดเจ็บเฉพาะที่ซึ่งอาจทำให้เกิดความกดดันภายในสมอง รอยโรคที่พบบ่อยที่สุดที่เกี่ยวข้องกับ TBI คือ hematomas และ contusions นอกจากนี้การบาดเจ็บที่สมองรวมถึงการบาดเจ็บแบบกระจายและกระดูกกะโหลกแตกด้วย
การวินิจฉัยโรค
เช่นเดียวกับผู้ป่วยบาดเจ็บทุกคน ผู้ที่บาดเจ็บที่ศีรษะจำเป็นต้องได้รับการประเมินอย่างเป็นระบบและรวดเร็วในห้องฉุกเฉิน โดยประเมินการทำงานของหัวใจและปอดก่อน ถัดไปจะทำการตรวจร่างกายอย่างรวดเร็วตามด้วยการตรวจทางระบบประสาทที่สมบูรณ์ การตรวจระบบประสาทรวมถึงการประเมินระดับการเปลี่ยนแปลงของความรู้สึกตัว โดยใช้ Glasgow coma scale (GCS) นอกเหนือจาก GCS ความสามารถของรูม่านตาที่จะกลายเป็นขนาดเล็กในแสงจ้าจะได้รับการทดสอบ และปฏิกิริยาของก้านสมอง รวมทั้ง ปฏิกิริยาสำรอกอาหารและปฏิกิริยาของแก้วตา (กะพริบตา) ก็อาจได้รับการทดสอบ
การทดสอบทางรังสีวิทยา
การสแกนเอกซ์เรย์คอมพิวเตอร์ (CT หรือ CAT scan) เป็น gold standard สำหรับการประเมินทางรังสีของผู้ป่วยบาดเจ็บที่ศีรษะ โดย CT scan นั้นใช้งานได้ง่ายและเป็นการทดสอบที่ยอดเยี่ยม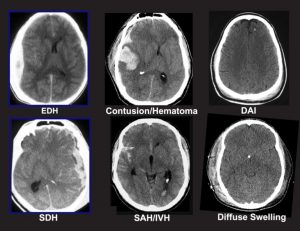 สำหรับการตรวจจับว่ามีเลือดและกระดูกหักซึ่งเป็นแผลที่สำคัญที่สุดในการวินิจฉัยในกรณีการบาดเจ็บทางการแพทย์ Plain x-rays of the skull ได้รับการแนะนำโดยบางคนว่าเป็นวิธีการหนึ่งในการประเมินผู้ป่วยที่มีความผิดปกติทางระบบประสาทที่ไม่รุนแรงเท่านั้น การถ่ายภาพด้วยคลื่นสนามแม่เหล็ก (MRI) ไม่ได้ใช้กันทั่วไปสำหรับการบาดเจ็บที่ศีรษะแบบเฉียบพลัน อย่างไรก็ตามหลังจากผู้ป่วยมีอาการคงที่ MRI อาจแสดงให้เห็นถึงการมีอยู่ของรอยโรคที่ไม่ถูกตรวจพบในการตรวจด้วย CT scan โดยทั่วไปข้อมูลนี้มีประโยชน์ในการวินิจฉัยโรคมากกว่าการรักษา
สำหรับการตรวจจับว่ามีเลือดและกระดูกหักซึ่งเป็นแผลที่สำคัญที่สุดในการวินิจฉัยในกรณีการบาดเจ็บทางการแพทย์ Plain x-rays of the skull ได้รับการแนะนำโดยบางคนว่าเป็นวิธีการหนึ่งในการประเมินผู้ป่วยที่มีความผิดปกติทางระบบประสาทที่ไม่รุนแรงเท่านั้น การถ่ายภาพด้วยคลื่นสนามแม่เหล็ก (MRI) ไม่ได้ใช้กันทั่วไปสำหรับการบาดเจ็บที่ศีรษะแบบเฉียบพลัน อย่างไรก็ตามหลังจากผู้ป่วยมีอาการคงที่ MRI อาจแสดงให้เห็นถึงการมีอยู่ของรอยโรคที่ไม่ถูกตรวจพบในการตรวจด้วย CT scan โดยทั่วไปข้อมูลนี้มีประโยชน์ในการวินิจฉัยโรคมากกว่าการรักษา
การผ่าตัดรักษา
ผู้ป่วยจำนวนมากที่มีอาการบาดเจ็บที่ศีรษะปานกลางหรือรุนแรงจะถูกนำส่งโดยตรงจากห้องฉุกเฉินไปที่ห้องผ่าตัด ในหลายกรณีการผ่าตัดจะทำเพื่อเอาเลือดหรือฟกช้ำที่มีขนาดใหญ่ออกซึ่งบีบอัดในสมองอย่างมีนัยสำคัญหรือเพิ่มแรงกดดันภายในกะโหลกศีรษะ หลังการผ่าตัดผู้ป่วยเหล่านี้มักจะถูกสังเกตและเฝ้าระวังอยู่ในหอผู้ป่วยหนัก
การรักษาทางการแพทย์
ในปัจจุบันยังไม่มียา หรือ “การรักษามหัศจรรย์” ที่สามารถให้การป้องกันความเสียหายแก่เส้นประสาท หรือส่งเสริมการรักษาเส้นประสาทหลังจากเกิดการบาดเจ็บที่ศีรษะ เป้าหมายหลักในห้องไอซียู คือ เพื่อป้องกันสมองบาดเจ็บระยะที่สอง โดย “primary insult” จะส่งผลให้เกิดการบาดเจ็บเบื้องต้นที่สมอง ในขณะที่ “secondary insult” คือ การพัฒนาใดๆ ที่ตามมา ซึ่งอาจนำไปสู่การบาดเจ็บทางระบบประสาท ยกตัวอย่าง เช่นสมองที่ได้รับบาดเจ็บจะมีความอ่อนไหวเป็นพิเศษ และมีความเสี่ยงต่อการลดของความดันโลหิตที่อาจทนได้ วิธีหนึ่งในการหลีกเลี่ยง secondary insults คือ การพยายามรักษาระดับความดันโลหิตให้เป็นปกติหรือสูงขึ้นเล็กน้อย ในทำนองเดียวกันการเพิ่มขึ้นของ ICP, การลดลงของออกซิเจนในเลือด, การเพิ่มอุณหภูมิของร่างกาย, การเพิ่มขึ้นของระดับน้ำตาลในเลือด และการรบกวนอื่น ๆ อีกมากมายที่อาจทำให้ระบบประสาทเสียหาย การป้องกัน secondary insults เป็นส่วนสำคัญของการจัดการห้องไอซียูของผู้ป่วยที่ได้รับบาดเจ็บที่ศีรษะ
ผลลัพธ์
หนึ่งในระบบที่ใช้กันอย่างแพร่หลายในการจำแนกผลลัพธ์จากการบาดเจ็บที่ศีรษะ คือ Glasgow Outcome Scale (GOS) ผู้ป่วยที่มีอาการบาดเจ็บที่ศีรษะเล็กน้อย (โดยปกติจะกำหนดเป็นคะแนน GCS 13-15) มีแนวโน้มที่จะดีขึ้น พวกเขาอาจยังมีอาการปวดหัว, วิงเวียน, หงุดหงิด หรือมีอาการคล้ายกัน แต่อาการเหล่านี้จะค่อยๆ ดีขึ้น
ผู้ป่วยที่มีอาการบาดเจ็บที่ศีรษะระดับปานกลางไม่ค่อยดีนัก ประมาณ 60 เปอร์เซ็นต์จะฟื้นตัวในเชิงบวก และประมาณ 25 เปอร์เซ็นต์ที่เหลือจะอยู่ในระดับปานกลางของความพิการ การเสียชีวิตหรือผู้ป่วยที่เป็นผักอยู่นานเกิน 1 เดือนจะเป็นผลลัพธ์ในประมาณ 7 ถึง 10 เปอร์เซ็นต์ของผู้ป่วยทั้งหมด ส่วนที่เหลือของผู้ป่วยจะมีระดับความพิการรุนแรง
การฟื้นฟู
เมื่อผู้ป่วยที่ได้รับบาดเจ็บที่ศีรษะออกจากโรงพยาบาลที่ดูแลเฉียบพลันแล้ว บางราย อาจได้รับประโยชน์จากโปรแกรมการฟื้นฟูสมรรถภาพ ผู้สมัครที่สำคัญสำหรับการฟื้นฟูสมรรถภาพก็คือ ผู้ป่วยที่มีอาการบาดเจ็บเบื้องต้นน้อยกว่าหรือผู้ที่เริ่มมีอาการดีขึ้นอย่างมีนัยสำคัญ ในบางกรณีการฟื้นฟูต่อไปอาจทำได้โดยการย้ายไปที่โรงพยาบาลสำหรับการฟื้นฟูสมรรถภาพ หรือไปยังบริการฟื้นฟูสมรรถภาพของโรงพยาบาลขนาดใหญ่
สำหรับผู้ป่วยที่ได้รับบาดเจ็บสาหัส หรือผู้ที่ฟื้นตัวช้า จำเป็นต้องมีการเฝ้าระวังอย่างต่อเนื่อง เพื่อป้องกันการเกิดปัญหาการเคลื่อนไหวของข้อต่ออย่างค่อยเป็นค่อยไป, ความสมบูรณ์ของผิวหนัง, ภาวะการหายใจ, การติดเชื้อและหน้าที่ทางสรีรวิทยาอื่นๆ ผู้ป่วยที่ได้รับบาดเจ็บปานกลางหรือไม่รุนแรง รวมถึงผู้ป่วยที่ได้รับบาดเจ็บอย่างรุนแรงซึ่งได้รับการฟื้นฟูอย่างเพียงพอ อาจเข้าร่วมสำหรับการรักษาแบบผู้ป่วยนอก
การป้องกัน
เพื่อลดความเสี่ยงของการบาดเจ็บที่สมอง คุณควรสวมเข็มขัดนิรภัยขณะขับขี่ ส่วนเด็กเล็กควรนั่งในเบาะนั่งสำหรับเด็กและติดตั้งในเบาะด้านหลัง นอกจากนี้คุณควรสวมหมวกนิรภัยเมื่อขี่มอเตอร์ไซค์, จักรยาน หรือขณะเล่นกีฬา เช่น สเก็ตบอร์ด, สโนว์โมบิลหรือยานพาหนะทุกพื้นที่ เพื่อป้องกันศีรษะในกรณีที่เกิดอุบัติเหตุ
● การป้องกันการหกล้ม สามารถช่วยให้ผู้สูงอายุหลีกเลี่ยงการหกล้มรอบบ้านได้เช่น การติดตั้งราวจับในห้องน้ำ, วางเสื่อกันลื่นในอ่างอาบน้ำหรือที่อาบน้ำ, การติดตั้งราวจับทั้งสองด้านของบันได, การปรับปรุงแสงสว่างในบ้าน, การจัดเก็บบันไดและพื้นไม่ให้มีของวางเกะกะ
● การป้องกันการบาดเจ็บที่ศีรษะในเด็ก เช่น ติดตั้งประตูนิรภัยที่ด้านบนของบันได, เก็บบันไดไม่ให้มีสิ่งของวางเกะกะ, ติดตั้งที่กั้นตรงหน้าต่างเพื่อป้องกันการตก, วางแผ่นกันลื่นในอ่างอาบน้ำหรือบริเวณที่อาบน้ำ, ใช้สนามเด็กเล่นที่มีวัสดุดูดซับแรงกระแทกที่พื้น, ตรวจสอบให้แน่ใจว่าบริเวณพื้นที่ที่ปูพรมนั้นปลอดภัย, อย่าให้เด็กเล่นบริเวณทางหนีไฟหรือระเบียง
- Published in Neurological Rehabilitation Center, Services
STROKE
What is Stroke?
Stroke is a medical emergency that occurs when blood supply to the brain is interrupted or cut off due to a blockage (ischemic stroke) or a rupture of the blood vessel (hemorrhagic stroke). Bleeding and deprivation of the brain from oxygen results in brain tissue damage and brain cell death. Stroke however, can be treated and prevented.
Current diagnostic methods are highly effective and are able to identify the location of the damage or abnormalities in the brain or blood vessels, as well as any conditions and causes that could be risk factors for an impending stroke.
What are the signs and symptoms of Stroke?
- Sudden numbness or weakness on one side of the body
- Sudden confusion
- Sudden difficulty in speaking or understanding speech
- Sudden vision impairment on one or both eyes
- Sudden trouble walking, dizziness or loss of balance
- Sudden severe headache with unknown cause
What is the role of Functional Medicine in Stroke?
Stroke is highly treatable and post-stroke patients have a high chance of recovering from complications and disabilities. Functional Medicine comes in to help improve one’s symptoms through a thorough investigation, holistic rehabilitation, biochemistry work up, nutritional enhancement, supportive therapies, and other possible treatments that aid in healing the actual brain injury. Stroke may also have a tendency to recur. Because of this, Functional Medicine enables patients with the necessary preventive knowledge and measures to boost their overall health considering their identified risk factors.
- Published in Neurological Rehabilitation Center, Services
Spina Bifida
- Published in Neurological Rehabilitation Center, Services
โรคพาร์กินสัน
โรคพาร์กินสันเป็นโรคความเสื่อมของระบบประสาทที่พบได้บ่อยในผู้สูงอายุ และมีผลให้มีปัญหาในเรื่องของอาการเคลื่อนไหวช้า(bradykinesia) หรืออาการเคลื่อนไหวได้น้อย (hypokinesia) การสั่น (tremor) อาการแข็งเกร็ง (rigidity) และยังมีอาการทรงตัวไมมั่นคง (postural instability) ร่วมด้วย
อาการและอาการแสดง
อาการและอาการแสดงของพาร์กินสัน ได้แก่:
● อาการสั่น หรืออาการสะบัด มักเริ่มต้นที่แขนขาบ่อยครั้งที่มือหรือนิ้วมือ โดยจะถูนิ้วโป้งและนิ้วชี้ไปมา เป็นที่รู้จักกันเรียกว่า การปั้นยาเม็ดลูกกลอน โดยมือจะสั่นขณะอยู่พัก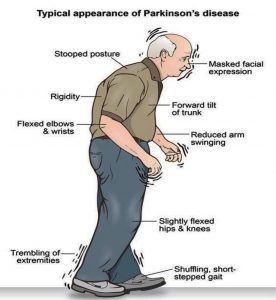
● การเคลื่อนไหวจะช้าลง เมื่อเวลาผ่านไปโรคพาร์กินสันจะทำให้การเคลื่อนไหวช้าลง ทำให้งานง่ายๆ ทำได้ยากและใช้เวลานานขึ้น การก้าวเดินจะสั้นลง ทำให้การลุกเดินออกจากเก้าอี้เป็นเรื่องยากและอาจลากเท้าเมื่อพยายามเดิน
● กล้ามเนื้อแข็งเกร็ง กล้ามเนื้อตึงอาจเกิดขึ้นที่ส่วนใดส่วนหนึ่งของร่างกาย กล้ามเนื้อตึงอาจทำให้รู้สึกเจ็บปวดและจำกัดการเคลื่อนไหวได้
● การบกพร่องของท่าทางและการทรงตัว ท่าทางอาจโค้งไปข้างหน้า หรือมีปัญหาการทรงตัวเนื่องจากโรคพาร์กินสัน
● การสูญเสียการเคลื่อนไหวอัตโนมัติ เช่น มีการลดความสามารถในการเคลื่อนไหวโดยไม่รู้ตัว รวมถึงการกระพริบตา การยิ้มหรือการแกว่งแขนขณะเดิน
● การพูดเปลี่ยนไป โดยอาจจะพูดเบาๆ, ช้าๆ, พูดไม่ชัดหรือลังเลก่อนพูด น้ำเสียงจะราบเรียบเป็นเสียงเดียวกันมากกว่าที่มีการผันตามปกติ
● การเขียนเปลี่ยนไป โดยเขียนหนังสือได้ลำบาก ตัวหนังสือจะค่อย ๆ เล็กลงจนอ่านไม่ออก
สาเหตุ
ในโรคพาร์กินสันเซลล์ประสาทบางส่วนในสมองจะค่อยๆ สลายหรือตายไป อาการหลายอย่างเกิดจากการสูญเสียเซลล์ประสาทที่ผลิตสารเคมีในสมองที่เรียกว่าโดปามีน เมื่อระดับโดปามีนลดลงมันจะทำให้เกิดการทำงานของสมองที่ผิดปกติซึ่งนำไปสู่อาการของโรคพาร์กินสัน สาเหตุของโรคพาร์กินสันยังไม่ทราบเป็นที่แน่ชัด แต่มีหลายปัจจัยที่มีบทบาทรวมไปถึง:
● พันธุกรรม
● ตัวกระตุ้นด้านสิ่งแวดล้อม
● การมี Lewy bodies
● การพบว่า Alpha-synuclein ภายใน Lewy bodies
ปัจจัยเสี่ยง
ปัจจัยเสี่ยงต่อการเกิดโรคพาร์กินสัน ได้แก่ :
● อายุ โดยผู้ใหญ่อายุน้อยมักไม่ค่อยมีโรคพาร์กินสัน โดยปกติจะเริ่มในช่วงกลางหรือปลายชีวิตและความเสี่ยงจะเพิ่มขึ้นตามอายุ โดยคนมักจะเป็นโรคนี้เมื่ออายุประมาณ 60 ปีขึ้นไป
● พันธุกรรม การมีญาติสนิทที่ป่วยเป็นโรคพาร์กินสันจะเพิ่มโอกาสที่คุณจะเป็นโรคนี้อย่างไรก็ตามความเสี่ยงของคุณยังคงมีน้อย เว้นแต่จะมีญาติหลายคนในครอบครัวของคุณมีโรคพาร์กินสัน
● เพศ โดยเพศชายมีแนวโน้มที่จะเป็นโรคพาร์กินสันได้มากกว่าเพศหญิง
● การสัมผัสกับสารพิษ เช่น การสัมผัสสารกำจัดวัชพืชและยาฆ่าแมลงอย่างต่อเนื่องอาจเพิ่มความเสี่ยงต่อการเกิดโรคพาร์กินสันได้
อาการแทรกซ้อน
โรคพาร์กินสันมักมาพร้อมกับปัญหาเพิ่มเติมเหล่านี้ซึ่งอาจรักษาได้: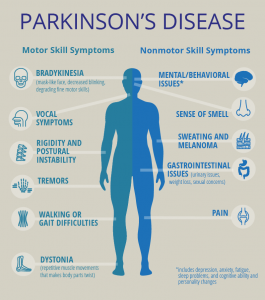
● ปัญหาด้านความคิด
● ภาวะซึมเศร้าและการเปลี่ยนแปลงทางอารมณ์
● ปัญหาการกลืน
● ปัญหาการเคี้ยวและกินอาหาร
● ปัญหาการนอนหลับและความผิดปกติของการนอนหลับ
● ปัญหาการขับปัสสาวะ
● ท้องผูก.
คุณอาจพบ:
● การเปลี่ยนแปลงของความดันโลหิต
● การดมกลิ่นที่ผิดปกติ
● ความเมื่อยล้า ความเจ็บปวด
● การเสื่อมสมรรถภาพทางเพศ
การวินิจฉัยโรค
ในขั้นต้นแพทย์จะประเมินโรคพาร์กินสันด้วยประวัติทางการแพทย์อย่างละเอียดและการตรวจระบบประสาท ผู้คนที่ได้รับยาลีโวโดปาพร้อมกับมีผลการปรับปรุงบางอย่างที่ดีขึ้นในด้านการเคลื่อนไหวซึ่งช่วยยืนยันการวินิจฉัย PD ส่วนสาเหตุอื่นที่ทำให้เกิดโรคพาร์กินสันเป็นครั้งที่สองคือโรคหลอดเลือดสมองและยาเสพติด
องค์กรทางการแพทย์ได้สร้างเกณฑ์การวินิจฉัยโรคเพื่อความสะดวกและเป็นมาตรฐานในกระบวนการวินิจฉัย โดยเฉพาะอย่างยิ่งในระยะแรกของโรค ได้กำหนดเกณฑ์ที่ต้องมีอาการเคลื่อนไหวช้า ร่วมกับอาการอย่างใดอย่างหนึ่งของอาการแข็งเกร็ง อาการสั่นขณะอยู่เฉย หรืออาการสูญเสียของการทรงตัว ส่วนสาเหตุที่เป็นไปได้อื่น ๆ ของอาการเหล่านี้จำเป็นต้องตัดออก ในที่สุดจำเป็นต้องใช้คุณสมบัติสนับสนุนอย่างน้อยสามอย่างต่อไปนี้ในระหว่างการดำเนินโรคหรือวิวัฒนาการ: อาการเริ่มข้างใดข้างหนึ่งก่อน, มีอาการสั่นขณะอยู่เฉย, อาการของโรคดำเนินมากขึ้นเรื่อยๆ, มีความไม่สมมาตรกันของการเคลื่อนไหว, มีการตอบสนองต่อยาลีโวโดปาอย่างน้อย 5 ปี, การดำเนินโรคทางคลินิกอย่างน้อย 10 ปี และ มีอาการยุกยิกเกิดจากการได้รับปริมาณยาลีโวโดปาที่มากเกินไป
การถ่ายภาพวินิจฉัย
การสแกนเอกซ์เรย์คอมพิวเตอร์ (CT) ของผู้ที่มี PD มักจะปรากฏเป็นปกติ ส่วน MRI จะมีความแม่นยำมากขึ้นในการวินิจฉัยโรคซึ่งสามารถแสดงให้เห็นถึงการขาดของลักษณะ ‘swallow tail’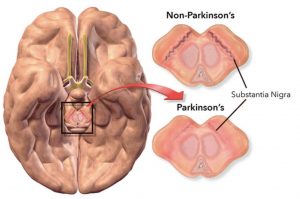 ที่เป็นรูปแบบการถ่ายภาพใน dorsolateral substantia nigra ในการวิเคราะห์อภิมานเกี่ยวกับการขาดของรูปแบบนี้มีความไวสูงและจำเพาะสำหรับโรค การทำ Diffusion MRI แสดงให้เห็นถึงความเป็นไปได้ในการแยกความแตกต่างระหว่าง PD และ Parkinson plus syndromes แม้ว่าค่าการวินิจฉัยยังอยู่ภายใต้การตรวจสอบ โดย CT และ MRI ยังคงใช้เพื่อแยกโรคอื่นๆ ที่อาจเป็นสาเหตุรองของโรคพาร์กินสันได้
ที่เป็นรูปแบบการถ่ายภาพใน dorsolateral substantia nigra ในการวิเคราะห์อภิมานเกี่ยวกับการขาดของรูปแบบนี้มีความไวสูงและจำเพาะสำหรับโรค การทำ Diffusion MRI แสดงให้เห็นถึงความเป็นไปได้ในการแยกความแตกต่างระหว่าง PD และ Parkinson plus syndromes แม้ว่าค่าการวินิจฉัยยังอยู่ภายใต้การตรวจสอบ โดย CT และ MRI ยังคงใช้เพื่อแยกโรคอื่นๆ ที่อาจเป็นสาเหตุรองของโรคพาร์กินสันได้
กิจกรรมการเผาผลาญของ dopamine transporters ใน basal ganglia สามารถวัดได้โดยตรงด้วยการสแกน PET และ SPECT ด้วย DaTSCAN ซึ่งแสดงให้เห็นถึงความเห็นด้วยอย่างยิ่งกับการวินิจฉัยทางคลินิกของโรคพาร์กินสัน กิจกรรมที่เกี่ยวข้องกับการลดลงของโดปามีนใน basal ganglia สามารถช่วยแยกกลุ่มอาการของยาที่ทำให้เกิดอาการคล้ายพาร์กินสัน การค้นพบนี้ไม่เฉพาะเจาะจงทั้งหมด อย่างไรก็ดีสามารถมองเห็นถึงความผิดปกติของทั้ง PD และ Parkinson-plus
การรักษา
โรคพาร์กินสันไม่สามารถรักษาให้หายขาดได้ แต่ยาสามารถช่วยควบคุมอาการได้บ่อยครั้งมาก ในบางกรณีอาจได้รับคำแนะนำเกี่ยวกับการผ่าตัด แพทย์อาจแนะนำการเปลี่ยนแปลงวิถีการดำเนินชีวิตโดยเฉพาะอย่างยิ่งการออกกำลังกายแบบแอโรบิค บางกรณีการทำกายภาพบำบัดที่เน้นเกี่ยวกับการทรงตัวและการยืดก็เป็นสิ่งสำคัญเช่นกัน นักอรรถบำบัดจะช่วยปรับปรุงปัญหาด้านการพูด
● ยา
ยาจะช่วยจัดการปัญหาเกี่ยวกับการเดิน, การเคลื่อนไหว และอาการสั่น โดยยาเหล่านี้จะช่วยเพิ่มหรือทดแทนโดปามีน คนที่เป็นโรคพาร์กินสันจะมีความเข้มข้นของโดปามีนในสมองต่ำ อย่างไรก็ตามโดปามีนไม่สามารถให้ได้โดยตรง เนื่องจากมันไม่สามารถเข้าสู่สมองของคุณได้ คุณจะมีอาการดีขึ้นอย่างมีนัยสำคัญหลังจากเริ่มรักษาโรคพาร์กินสัน อย่างไรก็ตามเมื่อเวลาผ่านไปประโยชน์ของยาบ่อยครั้งจะลดน้อยลงหรือกลายเป็นสอดคล้องกันน้อยลง คุณก็ยังคงสามารถควบคุมอาการของคุณได้ค่อนข้างดี
● ขั้นตอนการผ่าตัด
ในกระตุ้นสมองส่วนลึก ศัลยแพทย์จะทำการฝังอิเล็กโทรดเข้าไปในส่วนใดส่วนหนึ่งของสมอง ขั้วไฟฟ้าจะถูกเชื่อมต่อกับเครื่องกำเนิดไฟฟ้าที่ฝังอยู่ในหน้าอกใกล้กับกระดูกไหปลาร้าซึ่งจะส่งคลื่นไฟฟ้าไปยังสมอง และอาจช่วยลดอาการของโรคพาร์กินสันได้
● วิถีชีวิตและการเยียวยาที่บ้าน
หากคุณได้รับการวินิจฉัยว่าเป็นโรคพาร์กินสัน คุณจะต้องทำงานอย่างใกล้ชิดกับแพทย์ของคุณเพื่อหาแผนการรักษาที่ช่วยให้คุณบรรเทาได้มากที่สุดจากอาการที่มีผลข้างเคียงน้อยที่สุด แน่นอนว่าการเปลี่ยนแปลงวิถีการดำเนินชีวิตบางอย่างอาจช่วยให้การใช้ชีวิตกับโรคพาร์กินสันง่ายขึ้น
● การรับประทานอาหารเพื่อสุขภาพ
ในขณะนี้ยังไม่มีอาหาร หรือการรวมกันของอาหารที่ได้รับการพิสูจน์แล้วว่าช่วยในโรคพาร์กินสัน แต่อาหารบางชนิดอาจช่วยบรรเทาอาการบางอย่างได้ ตัวอย่างเช่น การกินอาหารที่มีเส้นใยสูงและดื่มน้ำในปริมาณที่เพียงพอสามารถช่วยป้องกันอาการท้องผูกที่พบได้บ่อยในโรคพาร์กินสัน อาหารสมดุลยังให้สารอาหาร เช่น กรดไขมันโอเมก้า 3 ที่อาจเป็นประโยชน์สำหรับผู้ที่เป็นโรคพาร์กินสัน
● การออกกำลังกาย
การออกกำลังกายจะช่วยเพิ่มความแข็งแรง, ความยืดหยุ่น และความสมดุลของกล้ามเนื้อ การออกกำลังกายยังช่วยปรับปรุงความเป็นอยู่ที่ดีของคุณและลดอาการซึมเศร้าหรือความวิตกังวล เช่น การเดิน, การว่ายน้ำ, การทำสวน, การเต้น, การเต้นแอโรบิกในน้ำ หรือการยืดกล้ามเนื้อ เป็นต้น
- Published in Neurological Rehabilitation Center, Services
Multiple Sclerosis
MULTIPLE SCLEROSIS (MS)
What is MS?
MS is an unpredictable autoimmune condition affecting the brain and spinal cord. The body attacks the protective sheath (myelin) that covers the nerve fibers. When the myelin sheath is damaged or destroyed, this can severely slow the process of transmitting information from the brain to the body. It can range from being benign
What are the signs and symptoms?
- Numbness or weakness in one or more limbs that typically occurs on one side of your body at a time, or the legs and trunk
- Electric-shock sensations that occur with certain neck movements
- Tremor, lack of coordination or unsteady gait
- Vision – partial or complete loss of vision (usually in one eye at a time), prolonged double vision, blurry vision
- Slurred speech
- Fatigue
- Dizziness
- Problems with sexual, bowel and bladder function
How is MS diagnosed?
There are no specific tests to diagnose MS but the doctor may rule out other conditions that have similar signs and symptoms. A series of tests and screening exams, medical history and thorough assessment helps in the diagnosis.
Role of Functional Medicine in MS
Functional Medicine is directed towards the underlying causes of the patient’s symptoms by addressing inflammation issues. The main goal is to enhance the body’s ability to care for itself and to support the immune system as a whole, reduce symptoms or delay the development of the disease.
The treatment plans vary per patient and their specific symptoms. Common approach would include nutritional assessment and revision of the patient’s diet, detect digestive problems and treat with FMT, eliminating possible toxins in the blood through antioxidants treatment, identifying infections, and appropriate physiotherapy activities.
- Published in Neurological Rehabilitation Center, Services
CEREBRAL PALSY (CP)
CEREBRAL PALSY (CP)
What is CP?
Cerebral Palsy is a combination of problems that affects ones muscle tone, movement and motor skills. A person with CP does not have coordination of movement. It can affect other basic but essential body functions such as breathing, bladder and bowel control, eating and talking. It often stems from brain damage that occurs before or during birth or from 3-5 years of a child’s life. Conditions like vision, hearing and learning problems may arise from CP. However, it does not progress or get worse over time.
What causes CP?
There is no definite cause. It happens during the brain’s development. It may be due to one factor or a combination of many issues. Some known factors that contribute to CP are:
- infections during pregnancy
- brain damage due to several causes such as injuries or meningitis
- complications in premature birth (poor blood flow to the brain)
- untreated jaundice
- mother’s medical problems during pregnancy
What are the types of CP?
- Spastic Cerebral Palsy — most common. Decreased muscle tone causes stiffness and jerky movements.
- Dyskinetic – characterized by uncontrolled movements that can be twisting, repetitive, slow, or unpredictable. Can be very severe.
- Ataxic – characterized by shaky movements that affects balance, coordination, posture positioning and even eye movements.
Role of Functional Medicine in CP
The goal in CP patients is to assist in improving brain and neurological function and improve symptoms. Integrative and customized neuro-regenerative programs are designed for each patient depending on their condition. Adjuvant therapies can also be identified and combined with our physiotherapy programs such as Robotics Training, G-Factor and Transcranial Magnetic Stimulation.
- Published in Neurological Rehabilitation Center, Services
Spinal bifida
Introduction: Spina bifida is a condition that affects the spine and is usually apparent at birth. It is a type of neural tube defect (NTD).
Spina bifida can happen anywhere along the spine if the neural tube does not close all the way. When the neural tube doesn’t close all the way, the backbone that protects the spinal cord doesn’t form and close as it should. This often results in damage to the spinal cord and nerves.
Spina bifida might cause physical and intellectual disabilities that range from mild to severe. The severity depends on:
- The size and location of the opening in the spine.
Whether part of the spinal cord and nerves are affected.
Causes of spina bifida
The cause of spina bifida is unknown, but a number of factors can increase the risk of a baby developing the condition.
These include:
- low folic acid intake during pregnancy
- having a family history of spina bifida
- medication – taking certain medications during pregnancy has been linked to an increased risk of having a baby with spina bifida
Sign and Symptom: Types of Spina Bifida
The three most common types of spina bifida are Myelomeningocele (sounds like: my-low-ma-nin-jo-seal; hear how “myelomeningocele” sounds
When people talk about spina bifida, most often they are referring to myelomeningocele. Myelomeningocele is the most serious type of spina bifida. With this condition, a sac of fluid comes through an opening in the baby’s back. Part of the spinal cord and nerves are in this sac and are damaged. This type of spina bifida causes moderate to severe disabilities, such as problems affecting how the person goes to the bathroom, loss of feeling in the person’s legs or feet, and not being able to move the legs.
Meningocele (sounds like: ma-nin-jo-seal; hear how “meningocele” sounds
Another type of spina bifida is meningocele. With meningocele a sac of fluid comes through an opening in the baby’s back. But, the spinal cord is not in this sac. There is usually little or no nerve damage. This type of spina bifida can cause minor disabilities.
Spina Bifida Occulta (sounds like: o-cult-tuh; hear how “occulta” sounds
Spina bifida occulta is the mildest type of spina bifida. It is sometimes called “hidden” spina bifida. With it, there is a small gap in the spine, but no opening or sac on the back. The spinal cord and the nerves usually are normal. Many times, spina bifida occulta is not discovered until late childhood or adulthood. This type of spina bifida usually does not cause any disabilities.
Diagnosis: Diagnosing spina bifida
Most cases of spina bifida are detected during the mid-pregnancy anomaly scan, which is offered to all pregnant women between 18 and 21 weeks of pregnancy.
If tests confirm that your baby has spina bifida, the implications will be discussed with you.
This will include a discussion about the possible problems associated with the condition, the treatment and support your child may need if you decide to continue with the pregnancy, and what your options are regarding ending the pregnancy, if that’s your choice.
Tests after birth
Once the baby is born, a number of tests may be carried out to assess the severity of the condition and help decide which treatments are appropriate.
Tests may include:
- monitoring your child’s head growth and carrying out a brain scan, using an ultrasound scan, CT scan or MRI scan, to check for hydrocephalus (excess fluid on the brain)
- ultrasound scans of the bladder and kidneys to check whether your baby stores urine normally
- an assessment of your baby’s movements to check for paralysis
In most cases, surgery to repair the spine will be recommended soon after your baby is born.
Treating spina bifida
Treatments for the symptoms or conditions associated with spina bifida include:
- surgery soon after birth to close the opening in the spine and treat hydrocephalus
- therapies to help make day-to-day life easier and improve independence, such as physiotherapy and occupational therapy
- assistive devices and mobility equipment, such as a wheelchair, or walking aids
- treatments for bowel and urinary problems
With the right treatment and support, many children with spina bifida survive well into adulthood.
It can be a challenging condition to live with, but many adults with spina bifida are able to lead independent and fulfilling lives.
Read more about treating spina bifida
Treatment: Treatments for the symptoms or conditions associated with spina bifida include:
- surgery soon after birth to close the opening in the spine and treat hydrocephalus
- therapies to help make day-to-day life easier and improve independence, such as physiotherapy and occupational therapy
assistive devices and mobility equipment, such as a wheelchair, or walking aids
- treatments for bowel and urinary problems
With the right treatment and support, many children with spina bifida survive well into adulthood.
It can be a challenging condition to live with, but many adults with spina bifida are able to lead independent and fulfilling lives.
What Makes our Treatment for Spina Bifida Effective?
Since 2005, we have been developing comprehensive stem cell therapy protocols for Spina Bifida to overcome the limitations of conventional therapies. In our protocols, stem cells are combined with specialized therapies for spina bifida that not only focus on helping the patient to cope with their symptoms, but also treat the root cause of the condition by promoting the healing of the original spinal cord/brain injury. We believe that our comprehensive therapy approach for spina bifida gives our patients the best chances of improvements, allowing for a better quality of life.
What potential improvements after the treatment?
The purpose of the treatment is to promote healing of the original spinal cord/brain injury in order to restore neurological function. Thus, various kinds of improvement are possible after our treatment and our past patients have experienced the following*:
- Improved motor function
- Increased sensations
- Improved development
- Improved mental abilities
- Increased muscle strength
- Reduced epilepsy seizures
- Enhanced bladder & bowel function
- Published in Neurological Rehabilitation Center, Services
Muscular Dystrophy
Introduction: Muscular dystrophy is a group of diseases that cause progressive weakness and loss of muscle mass. In muscular dystrophy, abnormal genes (mutations) interfere with the production of proteins needed to form healthy muscle.
There are many different kinds of muscular dystrophy. Symptoms of the most common variety begin in childhood, mostly in boys. Other types don’t surface until adulthood.
There’s no cure for muscular dystrophy. But medications and therapy can help manage symptoms and slow the course of the disease.
Causes
Muscular dystrophy is caused by mutations on the X chromosome. Each version of muscular dystrophy is due to a different set of mutations, but all prevent the body from producing dystrophin. Dystrophin is a protein essential for building and repairing muscles.
Duchenne muscular dystrophy is caused by specific mutations in the gene that encodes the cytoskeletal protein dystrophin. Dystrophin makes up just 0.002 percent of the total proteins in striated muscle, but it is an essential molecule for the general functioning of muscles.
Dystrophin is part of an incredibly complex group of proteins that allow muscles to work correctly. The protein helps anchor various components within muscle cells together and links them all to the sarcolemma – the outer membrane.
If dystrophin is absent or deformed, this process does not work correctly, and disruptions occur in the outer membrane. This weakens the muscles and can also actively damage the muscle cells themselves.
In Duchenne muscular dystrophy, dystrophin is almost totally absent; the less dystrophin that is produced, the worse the symptoms and etiology of the disease. In Becker muscular dystrophy, there is a reduction in the amount or size of the dystrophin protein.
The gene coding for dystrophin is the largest known gene in humans. More than 1,000 mutations in this gene have been identified in Duchenne and Becker muscular dystrophy
Sign and Symptom: The main sign of muscular dystrophy is progressive muscle weakness. Specific signs and symptoms begin at different ages and in different muscle groups, depending on the type of muscular dystrophy.
Duchenne type muscular dystrophy
This is the most common form of muscular dystrophy. Although girls can be carriers and mildly affected, it’s much more common in boys.
About one-third of boys with Duchenne muscular dystrophy (DMD) don’t have a family history of the disease, possibly because the gene involved may be subject to sudden abnormal change (spontaneous mutation).
Signs and symptoms typically appear in early childhood and may include:
- Frequent falls
- Difficulty rising from a lying or sitting up position
- Trouble running and jumping
- Waddling gait
- Large calf muscles
- Walking on the toes
- Muscle pain and stiffness
- Learning disabilities
Becker muscular dystrophy
Signs and symptoms are similar to those of Duchenne muscular dystrophy, but tend to be milder and progress more slowly. Symptoms generally begin in the teens but may not occur until the mid-20s or even later.
Other types of muscular dystrophy
Some types of muscular dystrophy are defined by a specific feature or by where in the body symptoms first begin. Examples include:
Facioscapulohumeral (FSHD). Muscle weakness typically begins in the face and shoulders. The shoulder blades might stick out like wings when a person with FSHD raises his or her arms. Onset usually occurs in the teenage years but may begin in childhood or as late as age 40
- Also known as Steinert’s disease, this form is characterized by an inability to relax muscles at will following contractions. Myotonic muscular dystrophy is the most common form of adult-onset muscular dystrophy. Facial and neck muscles are usually the first to be affected.
- Limb-girdle. Hip and shoulder muscles are usually the first affected. People with this type of muscular dystrophy may have difficulty lifting the front part of the foot and as a result may trip frequently. Onset usually begins in childhood or the teenage years..
- This type affects boys and girls and is apparent at birth or before age 2. Some forms progress slowly and cause only mild disability, while others progress rapidly and cause severe impairment.
Complications
The complications of progressive muscle weakness include:
- Trouble walking. Some people with muscular dystrophy eventually need to use a wheelchair.
- Shortening of muscles or tendons around joints (contractures). Contractures can further limit mobility.
- Breathing problems. Progressive weakness can affect the muscles associated with breathing. People with muscular dystrophy may eventually need to use a breathing assistance device (ventilator), initially at night but possibly also during the day.
- Curved spine (scoliosis). Weakened muscles may be unable to hold the spine straight.
- Heart problems. Muscular dystrophy can reduce the efficiency of the heart muscle.
- Swallowing problems. If the muscles involved with swallowing are affected, nutritional problems and aspiration pneumonia may develop. Feeding tubes may be an option.
Diagnosis: There are a variety of techniques used to definitively diagnose muscular dystrophy:
The genetic mutations involved in muscular dystrophy are well known and can be used to make a diagnosis.
- Enzyme assay: Damaged muscles produce creatine kinase (CK). Elevated levels of CK in the absence of other types of muscle damage could suggest muscular dystrophy.
- Genetic testing: As genetic mutations are known to occur in muscular dystrophy, these changes can be screened for.
- Heart monitoring: Electrocardiography and echocardiograms can detect changes in the musculature of the heart. This is especially useful for the diagnosis of myotonic muscular dystrophy.
- Lung monitoring: Checking lung function can give additional evidence.
- An electrode needle is inserted into the muscle to be tested. Electrical activity is measured as you relax and as you gently tighten the muscle. Changes in the pattern of electrical activity can confirm a muscle disease.
- Genetic testing. Blood samples can be examined for mutations in some of the genes that cause different types of muscular dystrophy.
- Muscle biopsy. A small piece of muscle can be removed through an incision or with a hollow needle. Analysis (biopsy) of the tissue sample can distinguish muscular dystrophies from other muscle diseases.
Treatment:
Drugs
The two most commonly prescribed drugs for muscular dystrophy are:
- Corticosteroids: This type of medication can help increase muscle strength and slow progression, but long-term use can weaken bones and increase weight gain.
Heart medications: If the condition impacts the heart, beta blockers and angiotensin-converting enzyme (ACE) inhibitors may help
Therapy
Several types of therapy and assistive devices can improve the quality and sometimes the length of life in people who have muscular dystrophy. Examples include:
- Range-of-motion and stretching exercises. Muscular dystrophy can restrict the flexibility and mobility of joints. Limbs often draw inward and become fixed in that position. Range-of-motion exercises can help to keep joints as flexible as possible.
- Low-impact aerobic exercise, such as walking and swimming, can help maintain strength, mobility and general health. Some types of strengthening exercises also might be helpful. But it’s important to talk to your doctor first because some types of exercise might be harmful.
- Braces can help keep muscles and tendons stretched and flexible, slowing the progression of contractures. Braces can also aid mobility and function by providing support for weakened muscles.
- Mobility aids. Canes, walkers and wheelchairs can help maintain mobility and independence.
- Breathing assistance. As respiratory muscles weaken, a sleep apnea device may help improve oxygen delivery during the night. Some people with severe muscular dystrophy may need to use a machine that forces air in and out of their lungs (ventilator).
What Makes our Stem Cell Treatment for Muscular Dystrophy Effective?
Since 2005, we have been developing comprehensive protocols regarding stem cell treatment for muscular dystrophy to overcome the limitations of conventional therapies. In our protocols, stem cells are combined with specialized therapies for muscular dystrophy that not only focus on helping the patient to cope with their symptoms, but also treat the direct cause of the symptoms by promoting the healing of the affected muscles. We believe that our comprehensive stem cell treatment for muscular dystrophy gives our patients the best chances of improvements, allowing for a better quality of life. Different types of muscular dystrophy can be considered for treatment, such as Duchenne, Becker, Limb Girdle, Fascio-Scapulo Humeral and more.
What potential improvements after therapy?
The purpose of stem cell treatment for muscular dystrophy is to promote the healing and growth of the affected muscles. Thus, various kinds of improvement are possible after our treatment and our past patients have experienced the following*:
- Enlarged muscle mass
- Improved range of movement
- Increased muscle strength
- Decreased tremor occurrence
- Improved balance
- Decreased stiffness
- Improved development (in children)
- Published in Neurological Rehabilitation Center, Services
Motor Neuron Diseases
MOTOR NEURON DISEASES (MNDs)
What is Motor Neuron Disease?
MNDs are a group of rare neurological disorders that progressively damage parts of the nervous system particularly the motor neurons. Motor Neurons are cells that control vital muscle activity responsible for gripping, speaking, walking, breathing and swallowing. This leads to general muscle weakness and is visible with wasting. A disruption in the signals between motor neurons and the muscles causes the dysfunction or loss of voluntary movement.
MNDs may affect children or adults. The causes of MNDs are not clearly known. It may be inherited, or effects of environmental, toxic, viral or a collection of many factors.
Signs and Symptoms:
There are numerous signs and symptoms and usually depend on the type of MND. Early signs and symptoms include:
- weakness in ankles or legs such as easily tripping or sudden difficulty to climb stairs
- slurred speech which gradually develop into difficulty swallowing some food
- weak hand grip manifested in dropping things or difficulty opening jars or buttoning clothes
- Weakness in shoulders that cause difficulty in lifting objects
- Unexplained muscle cramps and twitches
- weight loss or thinning of muscles on arms and legs
- breathing difficulty and shortness of breath not related to common respiratory disorders
Types of Motor Neuron Diseases
- ALS or Lou Gehrig’s disease – the most common type, affecting neurons in the brain and spinal cord. Effects are manifested on the muscles of the arms, legs, mouth, and respiratory system. A person with ALS may live another 3–5 years on avergae, but with proper supportive care, some have more than 10 years.
- Primary lateral sclerosis – rare form of MND that affects the neurons in the brain and progresses slower than ALS. It can still affect a person’s quality of life but is not fatal.
- Progressive bulbar palsy (PBP) – involves the brain stem. The condition causes frequent choking spells, difficulty speaking, eating, and swallowing.
- Progressive muscular atrophy (PMA) – a rare condition that affects the lower motor neurons in the spinal cord and causes slow but progressive muscle wasting, especially in the arms, legs, and mouth.
- Spinal muscular atrophy (SMA) – is an inherited MND that afflicts children caused by a genetic change known as SMA1. It usually affects the trunk, legs, and arms.
Role of Functional Medicine in MND
Functional Medicine for MND is multi-level assessment which usually starts with testing metabolic status, evaluating imbalances at the cellular level, genetic testing, identifying risk factors of the patient’s susceptibility to this disease and to help find out why the disease has occurred in the first place. By understanding each of the imbalances identified the specialist is able to formulate and educate the patient about the most appropriate and beneficial diet and lifestyle modification. Another purpose is to promote the healing of the brain injury which can manifest in improved motor functions, balance, better coordination, decreased fatigue, increase in muscle tone and strength, and other improvements of symptoms through intensive physiotherapy, Robotics training, possible stem cell treatment and FMT.
- Published in Neurological Rehabilitation Center, Services
- 1
- 2

 English
English  繁體中文
繁體中文  العربية
العربية  Português
Português  Español
Español